Absztrakt: Az oxidatív stressz a reaktív oxigénfajták termelése és a szervezet antioxidáns védelmi rendszere közötti egyensúlyhiányból adódik. Fontos szerepet játszik az immunválasz szabályozásában, és különböző betegségek kórokozója lehet. A krónikus rhinosinusitis (CRS) egy összetett és heterogén betegség, számos fenotípussal és endotípussal. A közelmúltban egyre több tanulmány utal arra, hogy az oxidatív stressz (mind a környezeti, mind a belső ingerek által okozott) fontos szerepet játszik a CRS patogenezisében és fennmaradásában. Ez több kutató figyelmét is felkeltette. A szabad gyökökből álló reaktív oxigénfajták jelenléte és az orrpolip patológiája közötti kapcsolat kulcsfontosságú, figyelmet érdemlő téma. Ez a cikk áttekinti az oxidatív stressz szerepét a légúti betegségekben, különösen a CRS-ben, és bemutatja a lehetséges terápiás antioxidánsokat, amelyek célzott kezelést kínálhatnak a CRS számára.
Junhu Tai1 , Jae-Min Shin1 , Jaehyung Park1 , Munsoo Han1,2 és Tae Hoon Kim1,2,*
Teljes angol nyelvű tanulmány letölthető
A fordítási hibákért elnézést kérek. Forrás: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC9854928/
Kulcsszavak: oxidatív stressz ; antioxidánsok; krónikus rhinosinusitis; nyálkahártya; a kutatás előrehaladása
1. Bevezetés
Az oxidatív stressz a reaktív oxigénfajták (ROS) termelése és lebomlása közötti egyensúlyhiányként definiálható [ 1 ]. Az aerob légzéssel történő energiatermelés során az ember és más emlősök különféle ROS-okat termelnek [ 2 ], például hidrogén-peroxidot és szuperoxid anionokat. A felesleges ROS különböző enzimek, köztük a szuperoxid-diszmutáz (SOD), a kataláz és más komponensek hatására eltávolítható, a normál tartományon belül tartandó. Oxidatív stressz esetén azonban a túlzott ROS szint sejtkárosodást okoz a fehérjékkel, lipidekkel és nukleinsavakkal való kölcsönhatások révén, ezáltal negatívan befolyásolja a szövetek működését és szerkezetét [ 3 ]. Különféle fiziológiai és kóros állapotok kapcsolódnak az oxidatív stresszhez; az antioxidáns rendszer kudarca és a fokozott ROS termelés összefüggésbe hozható az elhízással, az öregedéssel és néhány nyálkahártya-betegséggel [ 4 ]. Az utóbbi időben az oxidatív stressznek az emberi nyálkahártya rendszerére gyakorolt hatása egyre nagyobb figyelmet kapott a kutatóktól, különös tekintettel a légúti nyálkahártyára. Tanulmányok kimutatták, hogy a háziporatka képes ROS termelést indukálni, miközben gátolja az antioxidáns válaszokat a hörgőhámsejtekben [ 5 ]. Asztmás esetekben a ROS kulcsszerepet játszik a légúti gyulladások perzisztenciájában és felerősítésében, valamint elősegíti a nyálka hiperszekrécióját, a megnövekedett érpermeabilitást és a légutak átépülését [ 6 ]. Az alsó légutakra gyakorolt hatásukon túlmenően a ROS számos hatással van a felső légutak orrnyálkahártyájára is. Az orr nyálkahártya alatti mirigye több olyan molekula forrása, amelyek fontosak a nyálkahártya gazdaszervezet védelmében [ 7 ]. Az oxidatív stressz döntő szerepet játszhat az orr epiteliális gát diszfunkciójának vagy károsodásának előidézésében [ 8 ]. A krónikus sinusitis (CRS) egy olyan betegség, amely számos patogén tényezőből ered. Gyakori okai közé tartoznak a környezeti ingerek (például a környezetszennyezés); vírusos, gombás vagy bakteriális fertőzés; dohányzó; vagy fiziológiai tényezők, például genetikai hajlam és immunhiány [ 9 ]. A CRSwNP-ben szenvedő betegek számos szorongató tünettől szenvednek, beleértve az orrdugulást, a szaglás csökkenését vagy elvesztését, az orrfolyást, a hátsó orrfolyást és az arc nyomását vagy fájdalmát [ 10 ]. A közös 2-es típusú gyulladásos út eredményeként a CRSwNP-ben szenvedő betegek gyakran komorbid asztmában és/vagy nem szteroid gyulladáscsökkentő gyógyszerrel súlyosbított légúti betegségben szenvednek, ami miatt ismételt kortikoszteroid kezelésre és/vagy szinonasalis műtétekre van szükség a kontrollálatlan állapotok enyhítésére. tünetek [ 11 , 12]. A kezelés azonban gyakran nem hoz kielégítő eredményt, ami azt jelenti, hogy sürgősen új okokat és kezeléseket kell találni a CRSwNP-re. A CRSwNP kezelési lehetőségei közé tartozik az orvosi vagy sebészeti terápia, és a biológiai ágenseket jóváhagyták vagy a közelmúltban klinikai vizsgálatoknak vetették alá, de a CRSwNP kezelésére még nem hagytak jóvá antioxidánst [ 13 ]. Az emberi légúti nyálkahártya antioxidáns kapacitása fontos szerepet játszik a CRS, különösen az orrpolipokkal járó CRS (CRSwNP) etiológiájában [ 14 ]. A felső légutak veleszületett védekező mechanizmusának kulcstényezői közé tartozik a SOD, a peroxiredoxin-2 [ 15 ], a baktericid/permeabilitást növelő redőt tartalmazó család 1-es tagja (BPIFA1) [ 16 ] és az adenilát-ciklázt aktiváló polipeptid receptor 1. (ADCYAP1) [ 17 , 18 ].
Mivel a közvélemény ismeri a ROS következményeit, az emberek nagyon nagy elvárásokat támasztanak az antioxidánsokkal szemben, amelyek megakadályozhatják a ROS képződését. Az antioxidánsokban gazdag tápanyagokat általában kiegészítőként használják a ROS okozta károsodások csökkentésére [ 19 ]. Az antioxidánsok CRS-ben, különösen a CRSwNP-ben betöltött szerepével kapcsolatos legújabb tanulmányok elfogadható eredményeket erősítettek meg ebben a tekintetben. Például egy 32 CRS-ben szenvedő beteg bevonásával végzett vizsgálat megállapította, hogy az antioxidánsokkal végzett helyi kezelés jobb hatással volt a betegek orrüreg nyálkahártyájának műtét utáni helyreállítására, mint a többi hagyományos helyi kezelés [ 20 ]. Ez az áttekintés az oxidatív stressz szerepét tárgyalja a légúti betegségekben, különösen a CRS-ben. Kiemeljük továbbá a potenciális antioxidánsokat, amelyek felhasználhatók a CRS kezelésére, ahogy azt a legújabb kutatások is jelezték.
A tanulmány a PubMed, a Web of Science és a Scopus keresését végezte a következő keresési kifejezések kombinációjával (a címben/kivonatban): „krónikus orrnyálkahártya-gyulladás”, „oxidatív stressz” és „antioxidáns”. Ez az áttekintés nem korlátozta a kutatás típusait. Az alapkutatás és a klinikai kutatás egyaránt ide tartozik. A felvételi kritériumok közé tartoznak azok a cikkek, amelyek a CRSwNP, az oxidatív stressz és az antioxidánsok közötti kapcsolatot 1992 és 2022 között angol nyelven publikált alap- vagy klinikai kutatásokon keresztül tárják fel. Ezen túlmenően a cikkek típusára nincs korlátozás. A cikktípusok, mint például az áttekintés, az eredeti kutatás, a levelek, a közlemények és a vezércikkek, mind szerepelnek ebben az áttekintésben, és csak néhány olyan cikk került kizárásra, amelyek teljes szövege nem volt elérhető. Az összes kiválasztott cikk importálva lett az EndNote-ba, amely intelligensen törli az ismétlődő cikkeket.
2. Oxidatív stressz légúti betegségekben
A légzőrendszer összetett vezetőképes légutai és nagy alveoláris felülete miatt érzékeny az oxidatív stresszre [ 21 , 22 ]. A légúti oxidatív stresszt széles körben a légutak pro-oxidáns és antioxidáns folyamatai közötti egyensúlyhiányként definiálják [ 23 ]. A betegségeket okozó fő patogén tényezők közé tartoznak a fertőzések és gyulladások, a proteáz- és antiproteáz-egyensúly felborulása, valamint a szervezet antioxidáns védekezőképességét felülmúló oxidatív stressz [ 24 ]. A légúti betegségekben megnövekedett tüdő oxidatív stressz előfordulhat az exogén vagy endogén oxidánsok megnövekedett szintje vagy az endogén antioxidánsok csökkenése miatt.Asztal 1). Az exogén oxidálószerek közé tartozik a légszennyezés, a dohányfüst, a biomassza füstje, az allergének, a szemcsés anyagok és a finom szemcsés anyagok (<10 μ, <2,5 μ, <0,1 μ átmérőjű) [ 25 , 26 ]. Az endogén oxidánsok közé tartozik a hidrogén-peroxid, peroxinitrit, xantin-oxidáz, szuperoxid-anionok, mitokondriális oxidánsok és mieloperoxidáz [ 27 , 28 ]. Azok az antioxidánsok, amelyek csökkent szintet tapasztalhatnak a szervezetben: tioredoxin, nukleáris faktor eritroid 2-vel kapcsolatos 2. faktor (Nrf2), glutation, forkhead box protein, vitaminok és SOD [ 29 , 30 ]. Az oxidatív stressz számos mechanizmuson keresztül vezeti a légúti betegségeket, beleértve a proinflammatorikus transzkripciós faktor nukleáris faktor-κB (NF-κB) útvonalának aktiválását, a karbonilált fehérjékkel szembeni autoantitestek képződését, a sirtuin-1 csökkent expresszióját, a DNS-károsodást, az antiproteázok csökkent aktivitását és a transzformáló növekedési faktor-béta fokozott felszabadulása [ 31 ].
1. táblázat
| Exogén oxidálószerek | Endogén oxidálószerek | Csökkentett antioxidánsok |
|---|---|---|
| Légszennyeződés | Hidrogén-peroxid | tioredoxin |
| Dohányfüst | peroxinitrit | Nrf2 |
| Biomassza füst | Xantin-oxidáz | Glutation |
| Allergének | Szuperoxid anionok | Forkhead box protein |
| Részecske | Mitokondriális oxidánsok | Vitaminok |
| PM 2,5 (<10 μ, <2,5 μ, <0,1 μ) | Mieloperoxidáz | GYEP |
A légutak a külső környezettel való közvetlen érintkezési ablak. A szennyező vagy mérgező anyagok, mint például a nitrogén-dioxid, a kén-dioxid és a levegőben lévő részecskék asztmás tüneteket okozhatnak [ 32 ], és ezek az anyagok többé-kevésbé az oxidatív stresszel kapcsolatosak. Bizonyítékok vannak arra vonatkozóan, hogy az oxidatív stressz az asztma elterjedt tényezője [ 33 , 34 ]. Az antioxidáns-prooxidatív egyensúly felborulása kóros elváltozásokhoz vezethet a légúti hámsejtekben, és más betegségek (például légúti túlérzékenység) és az intracelluláris antioxidáns védelmi rendszer hibái hozzájárulhatnak az asztma kialakulásához [ 35 ]. Az oxidatív stresszhez kapcsolódó biomarkerek kimutatására szolgáló módszerek asztmában a kilégzett kondenzátum, a bronchoalveoláris folyadék, a szisztémás keringés és a vizelet vizsgálatát, valamint a kísérleti kimutatást tartalmazzák.2. táblázat).
2. táblázat
Az oxidatív stressz biológiai célpontjai és biomarkerei asztmában.
| Célok | Biomarkerek |
|---|---|
| Kilélegzett lehelet kondenzátum | Hidrogén ionok |
| Hidrogén-peroxid | |
| Nitrogén-oxid | |
| Nitrogén-oxidok | |
| 8-Izoprosztánok | |
| Glutation | |
| Bronchoalveoláris folyadék | 3-Brómotirozin |
| Kataláz | |
| Szisztémás keringés | Csökkentett glutation |
| C-vitamin | |
| α-tokoferol | |
| likopin | |
| β-karotin | |
| Vizelet | Bromotirozin |
| F2-izoprosztán | |
| Kísérleti észlelés | Réz-cink SOD |
| Mangán SOD |
A kilélegzett lehelet kondenzátumai és a hörgőfolyadék kimutatása a légúttal kapcsolatos módszerek számos, az oxidatív stresszel kapcsolatos biomarker kimutatására [ 36 , 37 ]. Azt találták, hogy az asztmás betegek leheletében a hidrogénionok, hidrogén-peroxid, nitrogén-oxid és 8-izoprosztán koncentrációja általában magasabb volt, mint az egészséges kontrollokban, és ezek az eredmények könnyen kimutathatók súlyos asztmában szenvedő betegeknél [38 ] . . 46 tanulmány áttekintése azt is feltárta, hogy a hidrogénionok, a hidrogén-peroxid és a nitrogén-monoxid koncentrációjának változása a kilégzett levegőben összefüggésben áll a gyermekek allergiás asztma állapotának súlyosbodásával [ 39 ]. A glutation szintje határozza meg, hogy a T helper típusú 1-es (Th1) vagy a 2-es típusú (Th2) immunválasz mód domináns, a glutation kimerülése pedig elősegíti a Th2-vel kapcsolatos reakciókat [ 40 ]. Az akut asztmás rohamok a glutation szintjének csökkenéséhez vezetnek a gyermekek kilélegzett lehelet kondenzátumaiban, és ezek a szintek szteroid kezelést követően emelkednek [ 41 ]. Egy tanulmány, amely az oxidánsok szerepét elemezte az emberi tüdőkárosodásban, azt találta, hogy az enyhe allergiás asztmában szenvedő egyének bronchoalveolaris folyadék fehérjéiben a 3-brómtirozin kiindulási szintje valamivel magasabb volt, mint a kontrollcsoporté; a szegmentális allergén kihívásnak való kitettség után ezen egyének bronchoalveoláris folyadékának 3-brómtirozin tartalma több mint 10-szeresére nőtt [ 42 ]. A kataláz enzim egy másik kulcsfontosságú antioxidáns. Aktivitása asztmás betegek bronchoalveolaris mosófolyadékában alacsonyabb, mint az egészséges kontrollokban, állatkísérletekben is hasonló megfigyelést tettek [ 43 ].
Az egyik tanulmányban az enzimatikus és nem enzimatikus antioxidánsok különböző komponenseit értékelték ELISA-val a glutation-peroxidáz és SOD enzimek szintjének értékelésére a betegek vérében, valamint nagy teljesítményű folyadékkromatográfiával a glutationszint-csökkenés mérésére [44 ] ; a glutation-peroxidáz és SOD szintje szignifikánsan alacsony volt az asztmás gyermekeknél. Egy másik tanulmány, amelyben 57 asztmás és 38 egészséges résztvevő vett részt, nem invazív módszerekkel vizsgálták az asztmával kapcsolatos markereket. A brótirozin és F2-izoprosztán vizeletszintje megemelkedett asztmás betegekben, ami azt jelzi, hogy ezek a vegyületek összefüggésbe hozhatók az asztmával [ 45 ]. Ami a kísérleti kimutatást illeti, a kutatók azt találták, hogy a redox-tiol/ditiol egyensúlyhiány megváltoztatja a réz-cink SOD szintjét az asztmás betegek sejtjeiben, és a réz-cink SOD-t a hidrogén-peroxid könnyen inaktiválja [ 46 ]. Az asztma egérmodelljében a réz-cink SOD transzgenikus egerek kevesebb légúti gyulladást és hiperreaktivitást mutattak [ 47 ].
A szennyező anyagok belélegzése megnöveli az asztmás egyének oxidatív terhelését, és a légúti hám oxidatív károsodása, valamint a veleszületett immunmechanizmusok aktiválódása allergiás szenzibilizációhoz és gyulladáshoz vezet. Ezen túlmenően az intracelluláris redox egyensúlyhiány a jelátviteli kaszkádok és a sejtválaszok megzavarását okozza, így fokozza a légúti gyulladást és elősegíti a légutak átépülését és a túlérzékenységet [ 48 ]. A kutatók N-acetilciszteint használnak a felesleges ROS eltávolítására és az endogén antioxidáns mechanizmusok elősegítésére. Sikeresen csökkentette a légúti gyulladást és a túlérzékenységet az asztma állatmodelljeiben, hasonlóan csökkentve a légúti túlérzékenységet egészséges emberekben és a dízel kipufogógáz részecskéknek kitett betegekben [ 49 , 50 ]. Más vizsgálatokban azonban az antioxidáns kezelések nem voltak hatással az asztmás tünetekre. A szulforafán kulcsszerepet játszik az oxidatív stressz és a gyulladás megelőzésében [ 51 ]. Egy 40 felnőtt bevonásával végzett kettős-vak, randomizált vizsgálat a szulforafán légúti gyulladásra és oxidatív stresszre gyakorolt hatását hasonlította össze [ 52 ]. A várttal ellentétben a szulforafán bevitel nem javította a tüdőgyulladás, az oxidatív stressz biomarkereinek vagy az asztma atópiájának klinikai jellemzőit. A jelenleg elérhető asztma és antioxidáns kezelések közötti kölcsönhatás tanulmányozása (például a kortikoszteroidok és a ROS közötti kölcsönhatásra összpontosítva) segíthet új terápiás beavatkozások kidolgozásában. A kortikoszteroid kezelés az asztmás betegek légúti oxidatív stresszének csökkentésével függ össze [ 53 ]. A hosszú távú kortikoszteroid kezelés azonban mitokondriális diszfunkcióhoz vezethet, ami ROS által közvetített kardiovaszkuláris, metabolikus és egyéb szövődményekhez vezet [ 54 , 55 ]. Bár az oxidatív stressz kezelésében nagy lehetőségek rejlenek az asztmaterápia segítésében, csak néhány tanulmány ért el sikereket e tekintetben, és a legtöbb kutatás nem tárt fel nyilvánvaló előnyöket.
Korábban áttekintettük az oxidatív stressz és az antioxidánsok hatását az allergiás rhinitisre, amely az asztmához hasonlóan egyesült légúti betegségnek számít. Az allergiás rhinitis egérmodelljébe és allergiás rhinitisben szenvedő betegek orrnyálkahártyájának hámsejtjébe transzkripciós faktorokat, például Nrf2-t és NF-κB-t vezettünk be. Számos lehetséges terápiás antioxidánst, például szulforafánt, resveratrolt és taurint is teszteltek, utóbbiak az oxidatív stressz markerek gátlásán keresztül ígéretes eredményeket mutattak [ 56 ]. A következő részben bemutatjuk az oxidatív stressz és az antioxidánsok szerepét egy másik egyesült légúti betegségben, a CRS-ben [ 57 ].
3. CRS és oxidatív stressz
3.1. A CRS endotípusa és fenotípusa
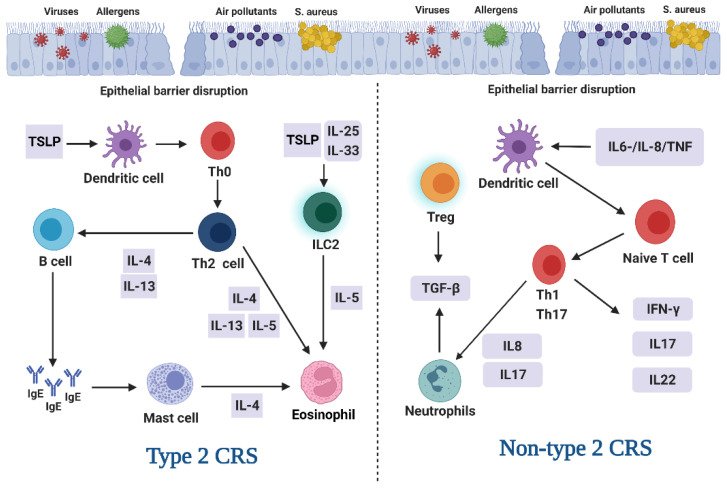
A CRS a Th1/Th17 és Th2 sejtek közötti immunválaszok különbségei alapján 2-es típusú és nem 2-es típusú CRS-be sorolható [ 58 ]. Korábbi tanulmányok arra a következtetésre jutottak, hogy az orrpolip nélküli CRS (CRSsNP) neutrofil túlsúlyt mutat, míg a CRSwNP eozinofil túlsúlyt mutat [ 59 ]. Azonban ezekkel az európai és amerikai betegekre vonatkozó megállapításokkal ellentétben a legtöbb CRSwNP-s ázsiai beteg neutrofil túlsúlyt mutatott, és a CRSsNP a 2-es típusú CRS-nek és az 1-es vagy 3-as típusú gyulladásnak kedvezõ immunválaszt mutatott [ 60 ]. Ahogy az ábrán látható1.ábra, a 2-es típusú CRS-re a hámsejtek rendellenessége és a Th2 sejtek (amelyek interleukin (IL)-4, IL-5 és IL-13 citokineket termelnek), B-sejtek, dendritikus sejtek és eozinofilek szintje emelkedett [61 , 62 ] . . Az orrmelléküreg epitélium a fő forrása a thymus stroma lymphopoietinjének, amely kulcsszerepet játszik a 2-es típusú gyulladásban a Th2 sejtek és a 2. csoportba tartozó veleszületett limfoid sejtek aktiválásával [ 63 ]. Az IL-5 elősegíti az eozinofil gyulladást, míg az IL-4 és IL-13 aktiválja a homotípusos transzformációt és a nyálkatermelést a CRSwNP-ben [ 61 ]; A B-sejtek IgE-t és más immunglobulinokat termelnek [ 62 ]. Arról is beszámoltak, hogy a 2-es típusú gyulladásos citokinek, az IL-25 és IL-33, amelyek más epiteliális forrásokból származnak, szintje emelkedett a 2-es típusú CRS-ben [ 64 ]. A 2-es típusú CRS-től eltérően a nem 2-es típusú CRS a Th1/Th17 sejtek számának jelentős növekedésével jár, ami az interferon (IFN)-γ, IL-8 és IL-17 citokinek emelkedett szintjének felel meg [65 ] . Az IL-6, IL-8 és a tumornekrózis faktor serkentik az IFN-γ és további IL-8 termelését a T-sejtek által, hogy erősítsék az immunválaszt; Az IL-8 ebbe a régióba toborozza a neutrofileket, amelyek több citokint szabadítanak fel, és a környezeti ingerekre adott epiteliális válasz a dendrites sejtek aktiválódásához vezet, ezáltal indukálja a Th1 és Th17 sejtek differenciálódását [ 66 ]. Fenotípusa szerint a CRS-t jelenleg vagy expresszáló vagy hiányzó orrpolipok (NP-k) kategóriába sorolják [ 67 ]. A kettő közül a CRSwNP-t általában a nyálkaszállításért és öntisztulásért felelős orrnyálkahártya rostjainak diszfunkciója kíséri, ami ahhoz vezet, hogy a csillós sejtek nem képesek kenni a hámot és eltávolítani a szennyeződéseket [ 68 ]. A felső légutak veleszületett védekező mechanizmusának ez a változása a CRSwNP etiológiájához kapcsolódik, a traktus antibakteriális és antioxidáns kapacitása a CRSwNP előrehaladtával fokozatosan csökken [ 69 ]. Az antioxidáns kapacitás csökkenésével együtt az oxidatív stressz döntő szerepet játszik a CRSwNP patogenezisében [ 70 , 71 ].
3.2. Oxidatív stressz krónikus sinusitisben NP-kkel
Az oxidatív stresszt kiváltó exogén tényezők CRS-ben (ahogy más légúti megbetegedéseknél is) a dohányfüst, az allergének és a finom részecskék [ 72 , 73 ]. Ezek az exogén oxidánsok csökkenthetik a légúti hámsejtek permeabilitását és elpusztíthatják az orrüreg hámgátját [ 74 ], végső soron oxidatív stresszt váltva ki (2. ábra). A gyulladásos kemokinek kulcsszerepet játszanak a gyulladás koordinálásában [ 75 ], és redox reakciók szabályozzák őket [ 76 ]. Az eotaxin-1, a CC kemokincsalád tagja, eozinofil toborzást és aktiválást indukál. Egy tanulmány eotaxin immunreaktivitást figyelt meg az NP-k epiteliális és endothel sejtjeiben [ 77 ]. Egy másik tanulmány kimutatta, hogy az eotaxin-1 kulcsszerepet játszik az eozinofilek szelektív toborzásában NP-kben [ 78 ]. A nikotinamidadenin-dinukleotid-foszfát (NADPH) oxidáz ROS-okat termel, amelyek részt vesznek az oxidatív stresszben és a jelátvitelben [ 79 ]. Egy nemrégiben készült tanulmány értékelte a NADPH oxidáz p67 phox alegységének és a 4-hidroxi-2-nonenál (4-HNE) oxidatív stressz marker expresszióját 13 CRSwNP-s beteg NP szöveteiben és kilenc egészséges kontroll orrnyálkahártyájában. Mindkettő expressziós szintje szignifikánsan magasabb volt az NP-szövetekben, mint az egészséges nyálkahártyákban [ 80 ], ami megerősíti, hogy az NP-szövetekben lipidperoxidáció történt. A tioredoxinnal kölcsönhatásba lépő fehérje (TXNIP) egy többfunkciós fehérje, amely a tioredoxin, egy antioxidáns aktivitásának gátlásával is növelheti a ROS termelést és oxidatív stresszt indukálhat [ 81 ]. Egy tanulmány megerősítette, hogy a TXNIP expressziója felfelé szabályozott CRSwNP-s betegekben, ami azt jelzi, hogy a fehérje kulcsszerepet játszik a CRSwNP patogenezisében [ 82 ]. A hem oxigenáz (HO)-1 citoprotektív enzim az oxidatív stressz ellen CRSwNP-ben [ 23 ]. Egy 40 CRSwNP-s beteg és 20 egészséges kontroll bevonásával végzett vizsgálatban a HO-1 mRNS és fehérjék expressziós szintje szignifikánsan magasabb volt a betegek NP-iben, mint a kontrollok orrnyálkahártyájában [ 83 ]. A scavenger receptorok felismerik az emberi szervezetbe behatoló különféle hulladékokat és idegen anyagokat, és általában ellensúlyozzák a környezeti toxinok által kiváltott ROS képződést [ 84 ]. A lektinszerű oxidált LDL receptor-1 (LOX-1) az egyik ilyen scavenger receptor, expresszióját az oxidatív stressz indukálja [ 85 ]. A LOX-1 mRNS expressziója szignifikánsan magasabb volt a CRSwNP-s betegekben, mint az egyik vizsgálat egészséges kontrolljaiban [ 86 ], hangsúlyozva a CRSwNP redox szabályozásában betöltött döntő szerepét.

A ROS neutrofil aktivációt okoz, ami felerősítheti a gének expresszióját, hogy felszabadítsa a megfelelő fehérjéket. E gének közül sok a transzkripciós faktorok, például az NF-κB aktiválásától függ az expresszió indukálása érdekében. Az NF-κB aktiváció lehet az alapja a humán neutrofil génexpresszió gyulladást elősegítő stimulációjának hatásának [ 87 ]. Az NP-k növekedése szorosan összefügg a különböző citokinek hatásaival is [ 88 ], és az NF-κB az egyik legfontosabb tényező a gyulladás során a citokinek termelődésével kapcsolatban. Egy tanulmány az NF-κB, a kapcsolódó gyulladásos citokinek és adhéziós molekulák expresszióját elemezte CRSwNP-s betegekben [ 89 ]. Egy CRSwNP csoport NP-i szignifikánsan több NF-κB p65-pozitív sejtet és magasabb mRNS-expressziós szintet tartalmaztak IL-6-ból, IL-8-ból és eotaxinból, mint a kontroll és a CRSsNP csoport uncinate szövetei. Az Nrf2 az oxidáció és a környezeti stressz kulcsfontosságú szabályozójaként működik azáltal, hogy a sejtmagba transzlokálódik, és elősegíti a sejtvédő választ kiváltó gének expresszióját [ 90 ]. Az orrüreg nyálkahártya gát funkciója és a szilárd részecskék által tönkretett csomópontok Nrf2 beadásával helyreállíthatók, ami azt jelzi, hogy az Nrf2 útvonal aktiválása a CRS potenciális terápiás célpontja lehet [ 91 ]. Egy másik tanulmány azt is kimutatta, hogy az orrüreg hámsejtek cigarettafüst által kiváltott barrier diszfunkciója a Nrf2 aktiválásával visszafordítható [ 92 ].
A fenti, CRSwNP-vel kapcsolatos oxidatív stresszreakciókon kívül a következőket jegyezték fel. A Ca2+/calmodulin-dependens protein kinase II (CaMKII) egy multipolimer szerin-treonin kináz [ 93 ]. A CaMKII normál aktivációja kiváltja az alegységek cseréjét ezen holoenzimek között, de a CaMKII ROS-on keresztüli fokozott aktivációja [ 94 , 95 ] gyulladáshoz és egyéb betegségekhez vezethet. A kinurenin/AhR tengely a hízósejtek aktivációját közvetíti az oxidatív CaMKII-n keresztül a CRSwNP patogenezisében [ 96 ]. Mélyebb kutatásra van szükség a kinurenin/AhR tengely és a CRSwNP-vel kapcsolatos oxidatív stressz közötti összefüggés tisztázásához.
A nyálkahártya felületét számos antibakteriális faktor védi, mint például a laktoperoxidáz, amely a ROS termelésén keresztül gátló hatást hoz létre a baktériumokon [ 97 ]. A laktoperoxidázhoz H 2 O 2 szükséges a tiocianát oxidálásához, így hipotiocianit termelődik [ 98 ]. Az epiteliális védekezés másik kulcsfontosságú folyamata a kettős oxigenáz (DUOX) expressziójának és működésének szabályozása [ 99 ]. Egy tanulmány, amely a DUOX1 expressziója és a gyulladásos mediátorok közötti összefüggést vizsgálta CRS-ben [ 100 ], azt találta, hogy a DUOX1 mRNS szintje szignifikánsan megemelkedett a CRSwNP-ben szenvedő betegekben az egészséges egyénekhez vagy a CRSsNP-s betegekhez képest. Valójában mind a CRSwNP, mind a CRSsNP csoport magasabb DUOX2 mRNS szintet mutatott, mint a kontrollcsoport. A H 2 O 2 tartalom szignifikánsan magas volt a CRSwNP-s betegekben, az orrváladék H 2 O 2 szintje szorosan összefügg a DUOX expressziós szintjével. Ezek az orrváladékok hasonlóan viszonylag magas citokinszintet mutattak, mint például az eotaxint, a tumornekrózis faktor-α-t és az IL-8-at. Ez a tanulmány kimutatta, hogy a ROS a DUOX1 és a DUOX2 túlzott expresszióját generálja CRSwNP-ben szenvedő betegekben, és a szerzők azt feltételezték, hogy a DUOX1 és DUOX2 kulcsfontosságú tényezők a veleszületett védekező jelátvitelben és az orrnyálkahártya-gyulladásban az emberi orr légúti epitéliumában.
Az ödéma fontos szövettani folyamat a CRSwNP patogenezisében. Az aktivált gyulladásos sejtek és a szekretált mediátoraik szöveti gyulladást és ödémát okoznak, és ennek a krónikus gyulladásos folyamatnak a hulladéka oxidatív stresszt okozó szabad gyököket tartalmaz [ 101 ]. Pontos szerepük és hatásuk a CRSwNP progressziójára azonban továbbra sem világos. Egy 24 CRSwNP-s beteg és 20 egészséges kontroll bevonásával készült vizsgálat az oxidatív állapot hatását vizsgálta a CRSwNP súlyosságára és a kapcsolódó életminőségi paraméterekre [ 102 ]. Az oxidatív stressz szint (a teljes antioxidáns státuszban és a nitrogén-szintben mérve) szignifikánsan összefüggött az orrdugulás mértékével és a betegség súlyosságával. Egy másik tanulmány a malondialdehid, a SOD és a nitrogén-monoxid koncentrációját hasonlította össze egészséges és NP szövetmintákban [ 70 ]. A kontroll szövetekhez képest az NP minták szignifikánsan magasabb malondialdehidet és alacsonyabb SOD-t és nitrogén-oxidot tartalmaztak. A lipid-peroxidáció fő végterméke a malondialdehid [ 103 ], míg az SOD és a nitrogén-oxid a legfontosabb antioxidánsok [ 104 ]. Ez szoros összefüggést mutatott az oxidatív stressz és az NP-k patogenezise között.
Az antioxidáns enzimek tekintetében a peroxiredoxin-2 (PRDX2), a BPIFA1 és az ADCYAP1 genetikai expressziója döntő jelentőségű a felső légutak veleszületett védekezési mechanizmusa szempontjából, a SOD mellett [ 69 ]. Egy 2006-ban végzett vizsgálatban az ADCAP1, BPIFA1 és SOD fehérjék szintjei eltérően expresszálódnak CRSwNP-ben és refrakter CRSwNP-ben szenvedő kínai betegek NP-iben, ami arra utal, hogy génjeik csökkent expressziós szintje összefüggésben lehet a patogenezissel. CRSwNP [ 105 ]. Emellett egy nemrégiben készült tanulmány arról számolt be, hogy az ADCYAP1, BPIFA1 és PRDX2 eltérően expresszálódott a CRSwNP-s kaukázusi betegek orrnyálkahártyájában [ 69 ], ami megerősítette, hogy e gének eltérő expressziója csökkentette az antioxidáns kapacitást a CRSwNP-ben szenvedő betegekben. És beszámoltak arról, hogy a PRDX2 összefüggésben áll az asztma súlyosságával, amely a CRSwNP egyik fő klinikai problémája [ 106 ]. Bár ugyanez a tanulmány megállapította, hogy a műtét és a hosszú távú lokális kortikoszteroid kezelés visszafordíthatja a fenti célgének expresszióját, ezekkel az eljárásokkal csak részben lehet enyhíteni az orrnyálkahártya antioxidáns kapacitásának csökkenését, és még mindig vannak hiányosságok az orrnyálkahártya antioxidáns kapacitásának visszaállításában. normál SOD homeosztázis. Ezenkívül számos műtét jelenti a CRSwNP-s betegek egyik fő klinikai problémáját, és a sebészeti kezelés nem lehet rutinszerű választás. Meg kell határozni az orrnyálkahártya antioxidáns kapacitását befolyásoló transzkripciós és szteroid-indukált változások hátterében álló specifikus mechanizmusokat. Bizonyíték van arra, hogy a foszfatáz és tenzin homológ gén (PTEN) gátolni tudja a foszfoinozitid 3-kináz (PI3K) aktiválódását, ami viszont befolyásolja a protein kináz B (Akt) foszforilációját [ 107 ]. A PI3K/PTEN/Akt jelátviteli út szabályozza a sejtnövekedést, az apoptózist, a proliferációt és az anyagcserét [ 108 ], és különféle krónikus gyulladásos és autoimmun betegségekhez kapcsolódik [ 109 ]. Egy in vitro vizsgálat a PTEN szerepét vizsgálta az orrhámsejtekben oxidatív stressz alatt, valamint a PTEN és a PI3K/Akt út közötti összefüggést [ 110 ]. Az egerek orrhámsejtjeit H 2 O 2 -vel kezeltük , hogy oxidatív stresszt váltsunk ki és sejtkárosodási modellt hozzunk létre. A H 2 O 2 által sérült sejtekben a ROS szint emelkedése és a megfelelő apoptózis miatt oxidatív stressz indukálódott, és ezt a károsodást különösen súlyosbította a PTEN. Az oxidatív stressz és a CRSwNP-vel kapcsolatos antioxidánsok vizsgálatait a cikk foglalja össze 3. táblázat, valamint az oxidatív stressz biomarkereit és a CRSwNP-vel kapcsolatos antioxidánsokat foglaljuk össze 4. táblázat.
3. táblázat
A CRSwNP-vel kapcsolatos oxidatív stressz és antioxidánsok vizsgálatainak összefoglalása.
| Kutatás típusa | Az alapkutatási tanulmány legfontosabb eredményei és a klinikai vizsgálat általános információi | Referencia |
|---|---|---|
| Alapkutatási tanulmányok | Eotaxin immunreaktivitás az NP-k endothel sejtjeiben | Yao et al. [ 77 ] |
| Az eotaxin-1 kulcsszerepet játszik az eozinofilek szelektív toborzásában az NP-kben | Yoshifuku et al. [ 78 ] | |
| A p67phox és a 4-HNE expressziója magasabb volt az NP szövetekben, mint az egészséges nyálkahártyákban | Zheng és mtsai. [ 80 ] | |
| A TXNIP expressziója felfelé szabályozott a CRSwNP-ben | Lin és mtsai. [ 82 ] | |
| A HO-1 mRNS és fehérjék expressziója magasabb volt az NP-ben, mint a kontrollban | Yu és mtsai. [ 83 ] | |
| A LOX-1 mRNS expressziója magasabb volt a CRSwNP-ben, mint az egészséges kontrollokban | Nishida et al. [ 86 ] | |
| A CRSwNP csoport több NF-κB p65-pozitív sejtet és magasabb IL-6, IL-8 és eotaxin mRNS expressziós szintet tartalmazott, mint a kontrollcsoport | Jung et al. [ 89 ] | |
| Az orr sinus epiteliális sejtjeinek barrier diszfunkciója az Nrf2 aktiválásával visszafordítható | Tharakan et al. [ 92 ] | |
| A DUOX1 mRNS szintje megemelkedett a CRSwNP-ben a kontrollhoz képest | Cho és mtsai. [ 100 ] | |
| Az oxidatív stressz szintje összefüggésben volt az orrdugulás és a betegség súlyosságával | Topal et al. [ 102 ] | |
| A kontroll szövetekhez képest az NP minták magasabb malondialdehidet és alacsonyabb SOD-t és nitrogén-oxidot tartalmaztak. | Cekin et al. [ 70 ] | |
| Klinikai vizsgálat | 25 kaukázusi beteg (10 nő és 15 férfi, 51-62 évesek). Közepes vagy magas preoperatív Malm endoszkópia és Lund–Mackay CT pontszámok. A kezelés 6 hónapig tartott | Mihalj et al. [ 69 ] |
4. táblázat
Az oxidatív stressz és az antioxidánsok biomarkerei a CRSwNP-ben.
| Az oxidatív stressz biomarkerei | Az antioxidánsok biomarkerei |
|---|---|
| Eotaxin-1 [ 77 , 78 ] | HO-1 [ 23 , 83 ] |
| NADPH [ 79 , 80 ] | LOX-1 [ 85 , 86 ] |
| TXNIP [ 81 , 82 ] | Nrf2 [ 90 , 91 , 92 ] |
| NF-κB [ 87 , 88 , 89 ] | SOD [ 70 , 102 , 104 ] |
| Laktoperoxidáz [ 97 , 98 ] | PRDX2 [ 69 , 111 ] |
| DUOX1, DUOX2 [ 99 , 100 ] | BPIFA1 [ 69 , 111 ] |
| Malondialdehid [ 70 , 102 , 103 ] | ADCYAP1 [ 69 , 111 ] PTEN, PI3K, Akt [ 107 , 108 , 109 , 110 ] |
3.3. Terápiás antioxidánsok krónikus rhinosinusitisben NP-kkel
Az oxidatív stressz fontos szerepet játszik az NP-k patogenezisében. A szabad gyökök által közvetített lipid-peroxidációs metabolitok magas szintjét figyelték meg az NP-k súlyosságával kapcsolatban [ 112 , 113 ]. Az oxidatív stressznek a CRSwNP előfordulására és kialakulására gyakorolt hatása alapján a kutatók feltárták a különféle antioxidánsok, köztük a flavonok, a resveratrol és a terpenoidok alkalmazhatóságát a betegség kezelésében. 5. táblázat).
5. táblázat
Potenciális antioxidánsok a CRS kezelésében.
| Antioxidánsok | Szerepek az orrnyálkahártyában és az NP-ben | Referencia |
|---|---|---|
| Számos reprezentatív flavon (apigenin, wogonin, krizin, tangeritin) | Gátolja a Muc5AC és az indukálható nitrogén-monoxid szintáz fokozódását, valamint a citokinek (pl. IL-8) felszabadulását | Hariri et al. [ 114 ] |
| Resveratrol | Csökkenti az eozinofil infiltráció és a subepiteliális fibrózis mértékét, valamint az IL-4, IL-5, a prosztaglandin D szintáz és a leukotrién C4 szintáz szintjét | Kim et al. [ 115 ] |
| Terpenoidok | A monoterpén-oxid 1,8-cineol csökkenti a túlzott eNOS foszforilációt, amely jellemzően az NP-kben található | Koennecke et al. [ 116 ] |
| kvercetin | Növeli a transzepiteliális Cl – transzportot és a ciliáris ütés gyakoriságát a szinonasalis epitélium tenyésztési modelljeiben | Zhang és mtsai. [ 117 ] |
| Erdostein | Ez a tanulmány összehasonlította a CRSwNP-ben szenvedő betegeket, akiket önmagában Erdosteinnel vagy Erdosteinnel és orrkortikoszteroid spray-vel kombinálva kezeltek, és azt találta, hogy a válasz szignifikánsan jobb volt a csak Erdosteinnel kezelt csoportban. | Hoza et al. [ 118 ] |
A flavonok bizonyítottan antioxidáns és gyulladáscsökkentő hatásúak [ 119 , 120 ]. Hariri et al. [ 110 ] azt találták, hogy számos flavon, például az apigenin, gátolja a Muc5AC és az indukálható nitrogén-monoxid-szintáz fokozódását, miközben gátolja a citokinek, például az IL-8 felszabadulását is. Ezek a hatások a légúti sejtek ciliáris verésének és mukociliáris clearance-ének növekedését eredményezték, alátámasztva a flavonok klinikai potenciálját, mint a CRSwNP terápiás lehetőségeit. Egy másik jelölt a resveratrol, amely egy perui hüvelyes növényből kivont természetes termék, amely erősen gátolja a ciklooxigenázt, hozzájárul a rák megelőzéséhez, és egyéb jótékony hatások mellett szív- és érrendszeri védelmet is nyújt [ 121 , 122 ]. Kim et al. eozinofil CRSwNP egérmodellt használt a rezveratrol terápiás hatásának tesztelésére, összehasonlítva a triamcinolon-acetoniddal; A rezveratrol szignifikánsan csökkentette az eozinofil infiltrációt és a subepiteliális fibrózis mértékét az egerek orrnyálkahártyájában, hasonlóan a triamcinolon-acetonid hatásához [ 111 ]. Ezenkívül az IL-4, IL-5, a prosztaglandin D szintáz és a leukotrién C4 szintáz expressziós szintjei szignifikánsan csökkentek a resveratrol kezelés hatására, és a resveratrol nagy dózisai erősen gátolták az 5-lipoxigenáz termelődését. Ezek az eredmények azt mutatják, hogy a resveratrol képes megelőzni és kezelni az eozinofil CRSwNP-t antioxidáns és gyulladáscsökkentő hatásai révén. A nitrogén-monoxid az orrban és az orrmelléküregekben szabadul fel, és a felső légúti betegségekhez kapcsolódik. Allergiás rhinitisben, CRSsNP-ben és CRSwNP-ben a nitrogén-monoxid koncentrációja megváltozik, és a betegség súlyosságának mutatójának tekintik [ 123 ]. Az endothel nitrogén-monoxid-szintáz (eNOS) fontos szerepet játszik a vaszkuláris permeabilitásban, az ödémában és a gyulladásban, a CRSwNP-ről pedig kimutatták, hogy fokozza az eNOS foszforilációját [ 116 ]. Az 1,8-Cineol egy természetes monoterpén, gyulladásgátló és antioxidáns tulajdonságokkal [ 124 ]. A kutatók azt találták, hogy az 1,8-cineol jelentősen befolyásolja az eNOS foszforilációját (és ezáltal annak későbbi aktiválódását), ami arra utal, hogy a terpenoid antioxidáció hatással lehet a CRSwNP kezelésére. A kvercetin egy másik erős antioxidáns hatással rendelkező bioaktív vegyület, amelyet alaposan tanulmányoztak [ 125 ]. Jelentősen növeli a transzepiteliális Cl – transzportot és a ciliáris szívverés gyakoriságát az egér és az emberi orr légúti sejtjeiben, bizonyítva a kvercetin alkalmazásának lehetőségét az orrmelléküregekbe történő helyi adagolásra [ 117]]. Egy másik kezelési lehetőség az erdostein, egy olyan gyógyszer, amelyet már jóváhagytak akut és krónikus tüdőbetegségek kezelésére, és eredetileg nyálkaoldó szerként fejlesztették ki. Antioxidáns, gyulladáscsökkentő és antibakteriális tulajdonságokkal rendelkezik, és a ROS termelés szabályozásával megelőzheti vagy csökkentheti az oxidatív stressz okozta tüdőszöveti károsodást [ 126 ]. Egy tanulmány értékelte az erdostein hatékonyságát a CRSwNP kezelésében, és azt találta, hogy a CRSwNP-ben szenvedő betegek endoszkópos eredményei és kérdőíves felmérési értékei javultak az erdostein-kezelés után, egy kontrollcsoporthoz képest. Ez megerősíti az erdostein alkalmazásának megvalósíthatóságát a jelenlegi gyógyszerek hatékony helyettesítőjeként [ 118 ].
4. Konklúziók
Áttekintettük az oxidatív stressz CRSwNP-re gyakorolt hatását leíró irodalmat, és összefoglaltunk néhány ígéretes antioxidánst a CRSwNP kezelésére. Azonban az antioxidánsok jelenlegi alkalmazása a CRSwNP-ben szenvedő betegeknél még mindig korlátozott, és nincs bizonyíték. Emellett az antioxidáns kezelések kutatásának akadályai és korlátai is vannak, például a klinikai esetek kis száma és a rövid kutatási idő. Jelenleg számos antioxidáns áll rendelkezésre a kutatók számára a hatékonyság értékeléséhez. A kulcs az, hogy ezt egy többközpontú, több populációra kiterjedő és többlépcsős vizsgálatban kell elvégezni. Egyszóval további mélyreható kutatások szükségesek a CRS-kezeléshez szükséges antioxidánsok fejlesztésének bizonyításához és támogatásához.
Finanszírozási nyilatkozat
Ezt a kutatást a Nemzeti Kutatási Alapítvány Alapvető Tudományos Kutatási Programja, a Tudományos és Technológiai Minisztérium, valamint a Koreai Tudományos, IKT- és Jövőtervezési Minisztérium finanszírozta (2017R1A2B2003575 és NRF-2020R1A2C1006398 támogatási szám). A tanulmányt az Információs és Kommunikációs Technológiai Tervezési és Értékelési Intézet felügyelte, és a Koreai Tudományos és ICT Minisztérium ICT Creative Consilience programja (IITP-2023-2020-0-01819) alá tartozik. Kutatásunkat a Koreai Egészségügyi Technológiai K+F Projekt (HI17C0387 és HR22C1302 támogatási szám) finanszírozta a Koreai Egészségügyi Iparfejlesztési Intézeten keresztül, amelyet az Egészségügyi és Jóléti Minisztérium kezel. Ezt a kutatást végül a Koreai Egyetem ösztöndíjából, valamint a Koreai Egyetemi Orvosi Központtól és a szöuli Anam Kórháztól kapott támogatásból finanszírozták.
Szerzői hozzájárulások
Írás – eredeti tervezet előkészítése; felülvizsgálat utáni javítások: JT; adatkezelés: JT és J.-MS; módszertan: JP és MH; áttekintés és szerkesztés: THK Minden szerző elolvasta és elfogadta a kézirat közzétett változatát.
Összeférhetetlenség
A szerzők nem nyilatkoznak összeférhetetlenségről.
Lábjegyzetek
Felelősség kizárása/Kiadói megjegyzés: Az összes publikációban szereplő nyilatkozatok, vélemények és adatok kizárólag az egyes szerző(k) és közreműködő(k) állításai, véleményei és adatai, nem pedig az MDPI-é és/vagy a szerkesztő(k)é. Az MDPI és/vagy a szerkesztő(k) kizárják a felelősséget a tartalomban hivatkozott ötletekből, módszerekből, utasításokból vagy termékekből eredő személyi vagy vagyoni sérülésekért.
Hivatkozások
1.
Cachofeiro V., Goicochea M., de Vinuesa SG, Oubiña P., Lahera V., Luño J. Oxidatív stressz és gyulladás, kapcsolat a krónikus vesebetegség és a szív- és érrendszeri betegségek között. Kidney Int. 2008; 74 :S4–S9. doi: 10.1038/ki.2008.516. [ PubMed ] [ CrossRef ] [ Google Scholar ]2.
Pieczenik SR, Neustadt J. Mitokondriális diszfunkció és a betegségek molekuláris útjai. Exp. Mol. Pathol. 2007; 83 , 84–92. doi: 10.1016/j.yexmp.2006.09.008. [ PubMed ] [ CrossRef ] [ Google Scholar ]3.
Tartaglia LA, Storz G., Ames BN Az oxiR-szabályozott promóterek azonosítása és molekuláris elemzése, amelyek fontosak az oxidatív stresszhez való bakteriális alkalmazkodáshoz. J. Mol. Biol. 1989; 210 , 709–719. doi: 10.1016/0022-2836(89)90104-6. [ PubMed ] [ CrossRef ] [ Google Scholar ]4.
Szewczyk-Golec K., Czuczejko J., Tylzanowski P., Lecka J. Strategies for Modulating Oxidative Stress under Diverse Physiological and Pathological Conditions. oxid. Med. Sejt. Longev. 2018; 2018 :3987941. doi: 10.1155/2018/3987941. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]5.
Wang Y., Bai C., Li K., Adler KB, Wang X. A légúti epiteliális sejtek szerepe az asztma és az allergiás nátha kialakulásában. Respir. Med. 2008; 102 , 949–955. doi: 10.1016/j.rmed.2008.01.017. [ PubMed ] [ CrossRef ] [ Google Scholar ]6.
Al-Harbi NO, Nadeem A., Al-Harbi MM, Ansari MA, AlSharari SD, Bahashwan SA, Attia SM, Al-Hosaini KA, Al Hoshani AR, Ahmad SF A légúti oxidatív stressz vaszkuláris és májgyulladást okoz a IL-17A az allergiás asztma egérmodelljében. Int. Immunopharmacol. 2016; 34 , 173–182. doi: 10.1016/j.intimp.2016.03.003. [ PubMed ] [ CrossRef ] [ Google Scholar ]7.
Peden DB, Brown ME, Wade Y., Raphael GD, Berkebile C., Kaliner MA Humán orrmirigy szekréciója új antioxidáns aktivitással: kolinerg kontroll. Am. Rev. Respir. Dis. 1991; 143 , 545–552. doi: 10.1164/ajrccm/143.3.545. [ PubMed ] [ CrossRef ] [ Google Scholar ]8.
Hong Z., Guo Z., Zhang R., Xu J., Dong W., Zhuang G., Deng C. Airborne Fine Particulate Matter Induces Oxidative Stress and Inflammation in Human Nasal Epithelial Cells. Tohoku J. Exp. Med. 2016; 239 , 117–125. doi: 10.1620/tjem.239.117. [ PubMed ] [ CrossRef ] [ Google Scholar ]9.
Kennedy DW A krónikus rhinosinusitis patogenezise. Ann. Otol. Rhinol. Laryngol. 2004; 193 , 6–9. doi: 10.1177/00034894041130S503. [ PubMed ] [ CrossRef ] [ Google Scholar ]10.
Bachert C., Bhattacharyya N., Desrosiers M., Khan AH. Betegség terhe krónikus orrpolipokkal járó rhinosinusitisben. J. Asztma allergia. 2021; 14 , 127–134. doi: 10.2147/JAA.S290424. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]11.
Fokkens WJ, Lund V., Bachert C., Mullol J., Bjermer L., Bousquet J., Canonica GW, Deneyer L., Desrosiers M., Diamant Z. és társai. Az EUFOREA konszenzusa a CRSwNP biológiai szerekről asztmával vagy anélkül. Allergia. 2019; 74 , 2312–2319. doi: 10.1111/all.13875. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]12.
Kim DW, Cho SH A krónikus rhinosinusitis feltörekvő endotípusai és alkalmazása a precíziós gyógyászatban. Allergia Asthma Immunol. Res. 2017; 9 , 299–306. doi: 10.4168/aair.2017.9.4.299. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]13.
Tai J., Han M., Kim TH. Biológiai terápiás stratégiák krónikus orrmelléküreg-gyulladásban: Jelenlegi lehetőségek és jövőbeli célok. Int. J. Mol. Sci. 2022; 23 :5523. doi: 10.3390/ijms23105523. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]14.
Kao SS, Bassiouni A., Ramezanpour M., Finnie J., Chegeni N., Colella AD, Chataway TK, Wormald PJ, Vreugde S., Psaltis AJ Egészséges és krónikus rhinosinusitisben szenvedő betegek orrnyálka-mintáinak proteomikai elemzése . J. Allergy Clin. Immunol. 2021; 147 , 168–178. doi: 10.1016/j.jaci.2020.06.037. [ PubMed ] [ CrossRef ] [ Google Scholar ]15.
Lu W., Fu Z., Wang H., Feng J., Wei J., Guo J. A peroxiredoxin 2 felszabályozott a vastagbélrákban, és hozzájárul a vastagbélráksejtek túléléséhez azáltal, hogy megvédi a sejteket az oxidatív stressztől. Mol. Sejt. Biochem. 2014; 387 , 261–270. doi: 10.1007/s11010-013-1891-4. [ PubMed ] [ CrossRef ] [ Google Scholar ]16.
Britto CJ, Cohn L. Baktericid/permeabilitást növelő fehérjeredőt tartalmazó családtag A1 légúti gazdavédelemben és légúti betegségekben. Am. J. Respir. Cell Mol. Biol. 2015; 52 , 525–534. doi: 10.1165/rcmb.2014-0297RT. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]17.
Yim SK, Kim KM, Lee CH, Song EK, Lee SO, Kim SW, Kim IH, Kim SH, Seo SY, Lee ST The Superoxide Dismutase Mimetic M40403, Javítja az 5-fluorouracil által kiváltott vékonybél nyálkahártyagyulladást egérmodellben . In Vivo. 2021; 35 , 1485–1497. doi: 10.21873/invivo.12401. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]18.
Bereswill S., Escher U., Grunau A., Kühl AA, Dunay IR, Tamas A., Reglodi D., Heimesaat MM Pituitary Adenylate Cyclase-Activating Polypeptide-A Neuropeptide as Novel Treatment Option for Subacute Ileitis in Mice Harboring a Emberi bélmikrobióta. Elülső. Immunol. 2019; 10 :554. doi: 10.3389/fimmu.2019.00554. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]19.
Seifried HE, Anderson DE, Fisher EI, Milner JA Áttekintés az étrendi antioxidánsok és a reaktív oxigénfajták közötti kölcsönhatásról. J. Nutr. Biochem. 2007; 18 , 567–579. doi: 10.1016/j.jnutbio.2006.10.007. [ PubMed ] [ CrossRef ] [ Google Scholar ]20.
Testa D., Marcuccio G., Panin G., Bianco A., Tafuri D., Thyrion FZ, Nunziata M., Piombino P., Guerra G., Motta G. Orrnyálkahártya gyógyulása endoszkópos sinus műtét után krónikus rhinosinusitisben idős betegek: A helyi alfa-tokoferol-acetát szerepe. Aging Clin. Exp. Res. 2017; 29 , 191–195. doi: 10.1007/s40520-016-0647-x. [ PubMed ] [ CrossRef ] [ Google Scholar ]21.
Arbex MA, Santos Ude P., Martins LC, Saldiva PH, Pereira LA, Braga AL Légszennyezés és a légzőrendszer. J. Bras. Pneumol. 2012; 38 , 643–655. doi: 10.1590/S1806-37132012000500015. [ PubMed ] [ CrossRef ] [ Google Scholar ]22.
Santus P., Corsico A., Solidoro P., Braido F., Di Marco F., Scichilone N. Oxidatív stressz és légzőrendszer: Az N-acetilcisztein farmakológiai és klinikai újraértékelése. COPD J. Chronic Obstr. Pulm. Dis. 2014; 11 , 705–717. doi: 10.3109/15412555.2014.898040. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]23.
Holguin F. Oxidatív stressz légúti betegségekben. Ann. Am. Thorac. Soc. 2013; 10 :S150–S157. doi: 10.1513/AnnalsATS.201305-116AW. [ PubMed ] [ CrossRef ] [ Google Scholar ]24.
Fischer BM, Voynow JA, Ghio AJ COPD: Oxidánsok és antioxidánsok kiegyensúlyozása. Int. J. Chronic Obstr. Pulm. Dis. 2015; 10 , 261–276. doi: 10.2147/COPD.S42414. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]25.
Mehta P., Bothiraja C., Mahadik K., Kadam S., Pawar A. Phytoconstituent based dry por inhalers as biomedicine for the management of pulmonary betegségek. Biomed. Pharmacother. 2018; 108 , 828–837. doi: 10.1016/j.biopha.2018.09.094. [ PubMed ] [ CrossRef ] [ Google Scholar ]26.
Gangwar RS, Bevan GH, Palanivel R., Das L., Rajagopalan S. Oxidative stress pathways of air pollution mediated toxicity: Recent insights. Redox Biol. 2020; 34 , 101545. old. doi: 10.1016/j.redox.2020.101545. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]27.
Hawkins CL, Davies MJ Az oxidatív fehérjemódosítások kimutatása, azonosítása és mennyiségi meghatározása. J. Biol. Chem. 2019; 294 , 19683–19708. doi: 10.1074/jbc.REV119.006217. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]28.
Ciencewicki J., Trivedi S., Kleeberger SR Oxidants and the pathogenesis of lung betegségek. J. Allergy Clin. Immunol. 2008; 122 , 456–468. doi: 10.1016/j.jaci.2008.08.004. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]29.
Hwang JW, Rajendrasozhan S., Yao H., Chung S., Sundar IK, Huyck HL, Pryhuber GS, Kinnula VL, Rahman I. A FOXO3-hiány fokozott érzékenységet eredményez a cigarettafüst által kiváltott gyulladásokra, a légtér megnagyobbodására és a krónikus obstruktív tüdőbetegség. J. Immunol. 2011; 187 , 987–998. doi: 10.4049/jimmunol.1001861. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]30.
Barnes PJ, Baker J., Donnelly LE Cellular Senescence as a Mechanism and Target in Chronic Lung Diseases. Am. J. Respir. Crit. Care Med. 2019; 200 , 556–564. doi: 10.1164/rccm.201810-1975TR. [ PubMed ] [ CrossRef ] [ Google Scholar ]31.
Barnes PJ Oxidatív stressz alapú terápia COPD-ben. Redox Biol. 2020; 33 , 101544. old. doi: 10.1016/j.redox.2020.101544. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]32.
Dozor AJ Az oxidatív stressz szerepe az asztma patogenezisében és kezelésében. Ann. NY Acad. Sci. 2010; 1203 , 133–137. doi: 10.1111/j.1749-6632.2010.05562.x. [ PubMed ] [ CrossRef ] [ Google Scholar ]33.
Comhair SA, Bhathena PR, Dweik RA, Kavuru M., Erzurum SC A szuperoxid-diszmutáz aktivitás gyors elvesztése az antigén által kiváltott asztmás válasz során. Gerely. 2000; 355 :624. doi: 10.1016/S0140-6736(99)04736-4. [ PubMed ] [ CrossRef ] [ Google Scholar ]34.
Dweik RA, Comhair SA, Gaston B., Thunnissen FB, Farver C., Thomassen MJ, Kavuru M., Hammel J., Abu-Soud HM, Erzurum SC NO kémiai események az emberi légutakban az azonnali és késői antigén során – kiváltott asztmás válasz. Proc. Natl. Acad. Sci. EGYESÜLT ÁLLAMOK. 2001; 98 , 2622–2627. doi: 10.1073/pnas.051629498. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]35.
Kleniewska P., Pawliczak R. Az oxidatív stressz részvétele a bronchiális asztma patogenezisében. Biomed. Pharmacother. 2017; 94 , 100–108. doi: 10.1016/j.biopha.2017.07.066. [ PubMed ] [ CrossRef ] [ Google Scholar ]36.
Cepelak I., Dodig S. Kilégzési kondenzátum: Új módszer a tüdőbetegségek diagnosztizálására. Clin. Chem. Labor. Med. 2007; 45 , 945–952. doi: 10.1515/CCLM.2007.326. [ PubMed ] [ CrossRef ] [ Google Scholar ]37.
Araneda OF, Carbonell T., Tuesta M. Frissítés az edzés által kiváltott tüdőgyulladás és oxidatív egyensúlyhiány mechanizmusairól. oxid. Med. Sejt. Longev. 2016; 2016 :4868536. doi: 10.1155/2016/4868536. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]38.
Aldakheel FM, Thomas PS, Bourke JE, Matheson MC, Dharmage SC, Lowe AJ Felnőttkori asztma és az oxidatív stressz markerek, valamint a kilélegzett levegő kondenzátum pH-értéke közötti kapcsolatok: szisztematikus áttekintés. Allergia. 2016; 71 , 741–757. doi: 10.1111/all.12865. [ PubMed ] [ CrossRef ] [ Google Scholar ]39.
Thomas PS, Lowe AJ, Samarasinghe P., Lodge CJ, Huang Y., Abramson MJ, Dharmage SC, Jaffe A. Kilélegzett lehelet kondenzátum gyermekgyógyászati asztmában: Ígéretes új előrelépés vagy hideg víz öntése sok forró levegőre? szisztematikus áttekintés. Pediatr. Pulmonol. 2013; 48 , 419–442. doi: 10.1002/ppul.22776. [ PubMed ] [ CrossRef ] [ Google Scholar ]40.
Peterson JD, Herzenberg LA, Vasquez K., Waltenbaugh C. A glutationszintek antigénprezentáló sejtekben modulálják a Th1 versus Th2 válaszmintákat. Proc. Natl. Acad. Sci. EGYESÜLT ÁLLAMOK. 1998; 95 , 3071–3076. doi: 10.1073/pnas.95.6.3071. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]41.
Corradi M., Folesani G., Andreoli R., Manini P., Bodini A., Piacentini G., Carraro S., Zanconato S., Baraldi E. Aldehydes and glutation in exhaled breath condensate of children with asthma exacerbation. Am. J. Respir. Crit. Care Med. 2003; 167 , 395–399. doi: 10.1164/rccm.200206-507OC. [ PubMed ] [ CrossRef ] [ Google Scholar ]42.
Wu W., Samoszuk MK, Comhair SA, Thomassen MJ, Farver CF, Dweik RA, Kavuru MS, Erzurum SC, Hazen SL Az eozinofilek brómozó oxidánsokat termelnek allergén által kiváltott asztmában. J. Clin. Investig. 2000; 105 , 1455–1463. doi: 10.1172/JCI9702. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]43.
Ghosh S., Masri F., Comhair S., Andreadis A., Swaidani S., Aronica M., Aulak K., Erzurum S. Fehérjék nitrálása az asztma egérmodelljében. Am. J. Respir. Crit. Care Med. 2003; 167 :A889. [ Google ösztöndíjas ]44.
Sackesen C., Ercan H., Dizdar E., Soyer O., Gumus P., Tosun BN, Büyüktuncer Z., Karabulut E., Besler T., Kalayci O. Az enzimatikus és nem enzimatikus antioxidáns rendszerek átfogó értékelése gyermekkori asztmában. J. Allergy Clin. Immunol. 2008; 122 , 78–85. doi: 10.1016/j.jaci.2008.03.035. [ PubMed ] [ CrossRef ] [ Google Scholar ]45.
Wedes SH, Khatri SB, Zhang R., Wu W., Comhair SA, Wenzel S., Teague WG, Israel E., Erzurum SC, Hazen SL A légúti gyulladás nem invazív markerei asztmában. Clin. Ford. Sci. 2009; 2 , 112–117. doi: 10.1111/j.1752-8062.2009.00095.x. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]46.
Comhair SA, Erzurum SC Az asztma redox kontrollja: Molekuláris mechanizmusok és terápiás lehetőségek. Antioxidáns. Redox jel. 2010; 12 , 93–124. doi: 10.1089/ars.2008.2425. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]47.
Larsen GL, White CW, Takeda K., Loader JE, Nguyen DD, Joetham A., Groner Y., Gelfand EW Azok az egerek, amelyek túlzottan expresszálják a Cu/Zn szuperoxid-diszmutázt, ellenállnak az allergén által kiváltott légúti szabályozási változásoknak. Am. J. Physiol. Tüdősejt. Mol. Physiol. 2000; 279 :L350–L359. doi: 10.1152/ajplung.2000.279.2.L350. [ PubMed ] [ CrossRef ] [ Google Scholar ]48.
Michaeloudes C., Abubakar-Waziri H., Lakhdar R., Raby K., Dixey P., Adcock IM, Mumby S., Bhavsar PK, Chung KF Az oxidatív stressz molekuláris mechanizmusai asztmában. Mol. Áspiskígyó. Med. 2022; 85 :101026. doi: 10.1016/j.mam.2021.101026. [ PubMed ] [ CrossRef ] [ Google Scholar ]49.
Shalaby KH, Allard-Coutu A., O’Sullivan MJ, Nakada E., Qureshi ST, Day BJ, Martin JG. A belélegzett nyírfa pollenkivonat oxidatív stresszen keresztül légúti túlérzékenységet vált ki, de függetlenül a pollenben rejlő NADPH-oxidáz aktivitástól vagy a TLR4-TRIF útvonal. J. Immunol. 2013; 191 , 922–933. doi: 10.4049/jimmunol.1103644. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]50.
Carlsten C., MacNutt MJ, Zhang Z., Sava F., Pui MM. Az antioxidáns N-acetilcisztein csökkenti a dízel kipufogógáz által kiváltott fokozott légúti reakcióképességet a légúti hiperreaktivitás esetén. Toxicol. Sci. 2014; 139 , 479–487. doi: 10.1093/toxsci/kfu040. [ PubMed ] [ CrossRef ] [ Google Scholar ]51.
Riedl MA, Saxon A., Diaz-Sanchez D. Az orális szulforafán növeli a II. fázisú antioxidáns enzimek szintjét az emberi felső légutakban. Clin. Immunol. 2009; 130 , 244–251. doi: 10.1016/j.clim.2008.10.007. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]52.
Sudini K., Diette GB, Breysse PN, McCormack MC, Bull D., Biswal S., Zhai S., Brereton N., Peng RD, Matsui EC Randomized Controlled Trial of the Effect of Broccoli Sprouts on Antioxidant Gene Expression és légúti gyulladás asztmás betegeknél. J. Allergy Clin. Immunol. Gyakorlat. 2016; 4 , 932–940. doi: 10.1016/j.jaip.2016.03.012. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]53.
Teng Y., Sun P., Zhang J., Yu R., Bai J., Yao X., Huang M., Adcock IM, Barnes PJ Hidrogén-peroxid kilégzett levegő kondenzátumában asztmában szenvedő betegeknél: Ígéretes biomarker? Mellkas. 2011; 140 , 108–116. doi: 10.1378/láda.10-2816. [ PubMed ] [ CrossRef ] [ Google Scholar ]54.
Luan G., Li G., Ma X., Jin Y., Hu N., Li J., Wang Z., Wang H. Dexamethasone-induced Mitochondrial Disfunction and Insulin Resistance-Study in 3T3-L1 Adipocytes and Mitochondria Egérmájból izolálva. Molekulák. 2019; 24 :1982. doi: 10,3390/molecules24101982. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]55.
Kračun D., Klop M., Knirsch A., Petry A., Kanchev I., Chalupsky K., Wolf CM, Görlach A. A NADPH-oxidázok és a HIF1 elősegítik a szívműködési zavarokat és a pulmonális hipertóniát válaszul a glükokortikoid feleslegre. Redox Biol. 2020; 34 , 101536. old. doi: 10.1016/j.redox.2020.101536. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]56.
Han M., Lee D., Lee SH, Kim TH Oxidative Stress and Antioxidant Pathway in Allergic Rhinitis. Antioxidánsok. 2021; 10 :1266. doi: 10.3390/antiox10081266. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]57.
Klain A., Indolfi C., Dinardo G., Licari A., Cardinale F., Caffarelli C., Manti S., Ricci G., Pingitore G., Tosca M. és társai. Egyesült légúti betegség. Acta Biomed. 2021; 92 :e2021526. doi: 10.23750/abm.v92iS7.12399. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]58.
Lee K., Tai J., Lee SH, Kim TH Advances in the Knowledge of the Underlying Airway Remodeling Mechanisms in Chronic Rhinosinusitis Based on the Endotypes: A Review. Int. J. Mol. Sci. 2021; 22 :910. doi: 10.3390/ijms22020910. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]59.
Van Zele T., Claeys S., Gevaert P., Van Maele G., Holtappels G., Van Cauwenberge P., Bachert C. A krónikus sinus betegségek differenciálása gyulladásos mediátorok mérésével. Allergia. 2006; 61 , 1280–1289. doi: 10.1111/j.1398-9995.2006.01225.x. [ PubMed ] [ CrossRef ] [ Google Scholar ]60.
Delemarre T., Holtappels G., De Ruyck N., Zhang N., Nauwynck H., Bachert C., Gevaert E. 2. típusú gyulladás krónikus rhinosinusitisben orrpolipok nélkül: Egy másik releváns endotípus. J. Allergy Clin. Immunol. 2020; 146 :337–343.e6. doi: 10.1016/j.jaci.2020.04.040. [ PubMed ] [ CrossRef ] [ Google Scholar ]61.
Shi LL, Song J., Xiong P., Cao PP, Liao B., Ma J., Zhang YN, Zeng M., Liu Y., Wang H. és társai. A léziós dendrites sejtek betegség-specifikus T-helper sejt polarizáló funkciója különböző típusú krónikus rhinosinusitisben orrpolipokkal. Am. J. Respir. Crit. Care Med. 2014; 190 , 628–638. doi: 10.1164/rccm.201402-0234OC. [ PubMed ] [ CrossRef ] [ Google Scholar ]62.
Klingler AI, Stevens WW, Tan BK, Peters AT, Poposki JA, Grammer LC, Welch KC, Smith SS, Conley DB, Kern RC és mások. A gyulladásos endotípusok mechanizmusai és biomarkerei krónikus rhinosinusitisben orrpolipok nélkül. J. Allergy Clin. Immunol. 2021; 147 , 1306–1317. doi: 10.1016/j.jaci.2020.11.037. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]63.
Kato A. A krónikus rhinosinusitis immunpatológiája. Allergol. Int. 2015; 64 , 121–130. doi: 10.1016/j.alit.2014.12.006. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]64.
Ogasawara N., Klingler AI, Tan BK, Poposki JA, Hulse KE, Stevens WW, Peters AT, Grammer LC, Welch KC, Smith SS és társai. A 2-es típusú gyulladás epiteliális aktivátorai: A thymus stroma limfopoietinszintjének emelkedése, de nem az IL-25 vagy IL-33, krónikus orrpolipokkal járó rhinosinusitisben Chicagóban, Illinois államban. Allergia. 2018; 73 , 2251–2254. doi: 10.1111/all.13552. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]65.
Zhang N., Van Zele T., Perez-Novo C., Van Bruaene N., Holtappels G., DeRuyck N., Van Cauwenberge P., Bachert C. A T-effektor sejtek különböző típusai irányítják a nyálkahártya gyulladását krónikus betegségben sinus betegség. J. Allergy Clin. Immunol. 2008; 122 , 961–968. doi: 10.1016/j.jaci.2008.07.008. [ PubMed ] [ CrossRef ] [ Google Scholar ]66.
Grayson JW, Hopkins C., Mori E., Senior B., Harvey RJ A krónikus rhinosinusitis kortárs osztályozása a polipokon túl a polipok nélkül: áttekintés. JAMA Otolaryngol. Head Neck Surg. 2020; 146 , 831–838. doi: 10.1001/jamaoto.2020.1453. [ PubMed ] [ CrossRef ] [ Google Scholar ]67.
Cho SH, Hamilos DL, Han DH, Laidlaw TM Phenotypes of Chronic Rhinosinusitis. J. Allergy Clin. Immunol. Gyakorlat. 2020; 8 , 1505–1511. doi: 10.1016/j.jaip.2019.12.021. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]68.
Olszewska A., Niewiadomski P., Olszewski J. Az orrnyálkahártya irritáló szerek hatása a krónikus rhinosinusitis előfordulására polipok nélkül/és polipokkal. Otolaryngol. Pol. 2021; 75 , 36–44. doi: 10.5604/01.3001.0014.2047. [ PubMed ] [ CrossRef ] [ Google Scholar ]69.
Mihalj H., Butković J., Tokić S., Štefanić M., Kizivat T., Bujak M., Baus Lončar M., Mihalj M. Expression of Oxidative Stress and Inflammation-Related Genes in Nasal Mucosa and Nasal Polyps from Krónikus rhinosinusitisben szenvedő betegek. Int. J. Mol. Sci. 2022; 23 :5521. doi: 10.3390/ijms23105521. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]70.
Cekin E., Ipcioglu OM, Erkul BE, Kapucu B., Ozcan O., Cincik H., Gungor A. Az oxidatív stressz és az orrpolipózis kapcsolata. J. Int. Med. Res. 2009; 37 , 325–330. doi: 10.1177/147323000903700206. [ PubMed ] [ CrossRef ] [ Google Scholar ]71.
Bozkus F., San I., Ulas T., Iynen I., Yesilova Y., Guler Y., Aksoy N. Az összes oxidatív stressz paramétereinek értékelése orrpolipokban szenvedő betegeknél. Acta Otorhinolaryngol. Ital. 2013; 33 , 248–253. [ PMC ingyenes cikk ] [ PubMed ] [ Google Scholar ]72.
Lee WH, Hong SN, Kim HJ, Ahn S., Rhee CS, Lee CH, Kim JW A cigarettázás hatásai orrgyógyászati betegségekre: Koreai Nemzeti Egészségügyi és Táplálkozási Vizsgálati Felmérés 2008–2011. Int. Fórum Allergia Rhinol. 2015; 5 , 937–943. doi: 10.1002/alr.21553. [ PubMed ] [ CrossRef ] [ Google Scholar ]73.
Mady LJ, Schwarzbach HL, Moore JA, Boudreau RM, Tripathy S., Kinnee E., Dodson ZM, Willson TJ, Clougherty JE, Lee SE A légszennyező anyagok környezeti kockázati tényezők lehetnek a krónikus rhinosinusitis betegség progressziójában. Int. Fórum Allergia Rhinol. 2018; 8 , 377–384. doi: 10.1002/alr.22052. [ PubMed ] [ CrossRef ] [ Google Scholar ]74.
Rusznak C., Sapsford RJ, Devalia JL, Justin John R., Hewitt EL, Lamont AG, Wood AJ, Shah SS, Davies RJ, Lozewicz S. A cigarettafüst felerősíti a háziporatka allergén által kiváltott emberi permeabilitásának növekedését hörgőhámsejtek in vitro. Am. J. Respir. Cell Mol. Biol. 1999; 20 , 1238–1250. doi: 10.1165/ajrcmb.20.6.3226. [ PubMed ] [ CrossRef ] [ Google Scholar ]75.
Taub DD, Oppenheim JJ. A kemokinek áttekintése a Third International Symposium of Chemotactic Cytokines konferencián. Citokin. 1993; 5 , 175–179. doi: 10.1016/1043-4666(93)90001-L. [ PubMed ] [ CrossRef ] [ Google Scholar ]76.
Sozzani S., Bosisio D., Mantovani A., Ghezzi P. Linking stress, oxidation and the chemokin system. Eur. J. Immunol. 2005; 35 , 3095–3098. doi: 10.1002/eji.200535489. [ PubMed ] [ CrossRef ] [ Google Scholar ]77.
Yao T., Kojima Y., Koyanagi A., Yokoi H., Saito T., Kawano K., Furukawa M., Kusunoki T., Ikeda K. Eotaxin-1, -2 és -3 immunreaktivitás és fehérje koncentrációja az eozinofil krónikus rhinosinusitises betegek orrpolipjaiban. Gégetükör. 2009; 119 , 1053–1059. doi: 10.1002/lary.20191. [ PubMed ] [ CrossRef ] [ Google Scholar ]78.
Yoshifuku K., Matsune S., Ohori J., Sagara Y., Fukuiwa T., Kurono Y. Az IL-4 és a TNF-alfa megnövelte az eotaxin szekrécióját az eozinofil beszűrődéssel járó orrpolipok tenyésztett fibroblasztjaiból. Rhinology. 2007; 45 , 235–241. [ PubMed ] [ Google Scholar ]79.
Brandes RP, Weissmann N., Schröder K. Nox család NADPH oxidázok: Az aktiválás molekuláris mechanizmusai. Free Radic. Biol. Med. 2014; 76 , 208–226. doi: 10.1016/j.freeradbiomed.2014.07.046. [ PubMed ] [ CrossRef ] [ Google Scholar ]80.
Zheng K., Hao J., Xiao L., Wang M., Zhao Y., Fan D., Li Y., Wang X., Zhang L. Nikotinamid-adenin-dinukleotid-foszfát-oxidáz expressziója krónikus rhinosinusitisben orrpolipokkal . Int. Fórum Allergia Rhinol. 2020; 10 , 646–655. doi: 10.1002/alr.22530. [ PubMed ] [ CrossRef ] [ Google Scholar ]81.
Alhawiti NM, Al Mahri S., Aziz MA, Malik SS, Mohammad S. TXNIP in Metabolic Regulation: Physiological Role and Therapeutic Outlook. Curr. Kábítószer célpontok. 2017; 18 , 1095–1103. doi: 10.2174/1389450118666170130145514. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]82.
Lin H., Ba G., Tang R., Li M., Li Z., Li D., Ye H., Zhang W. Increased Expression of TXNIP Facilitates Oxidative Stress in Nasal Epithelial Cells of Patiens With Chronic Rhinosinusitis with Orrpolipok. Am. J. Rhinol. Allergia. 2021; 35 , 607–614. doi: 10.1177/1945892420982411. [ PubMed ] [ CrossRef ] [ Google Scholar ]83.
Yu Z., Wang Y., Zhang J., Li L., Wu X., Ma R., Han M., Xu G., Wen W., Li H. A hem oxigenáz-1 expressziója eosinophilic és nem eozinofil krónikus rhinosinusitis orrpolipokkal: Citokinek általi moduláció. Int. Fórum Allergia Rhinol. 2015; 5 , 734–740. doi: 10.1002/alr.21530. [ PubMed ] [ CrossRef ] [ Google Scholar ]84.
Li N., Hao M., Phalen RF, Hinds WC, Nel AE Particulate air pollutants and asthma. Az oxidatív stressz szerepének paradigmája a PM által kiváltott káros egészségügyi hatásokban. Clin. Immunol. 2003; 109 , 250–265. doi: 10.1016/j.clim.2003.08.006. [ PubMed ] [ CrossRef ] [ Google Scholar ]85.
Sawamura T., Kume N., Aoyama T., Moriwaki H., Hoshikawa H., Aiba Y., Tanaka T., Miwa S., Katsura Y., Kita T. és társai. Az oxidált kis sűrűségű lipoprotein endothel receptora. Természet. 1997; 386 , 73–77. doi: 10.1038/386073a0. [ PubMed ] [ CrossRef ] [ Google Scholar ]86.
Nishida M., Takeno S., Takemoto K., Takahara D., Hamamoto T., Ishino T., Kawasumi T. A Lectin-Like Oxidized LDL Receptor-1 (LOX-1) fokozott szöveti expressziója a betegséggel kapcsolatos Súlyossága orrpolipokkal járó krónikus rhinosinusitisben. Diagnosztika. 2020; 10 :246. doi: 10.3390/diagnostics10040246. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]87.
McDonald PP, Bald A., Cassatella MA Az NF-kappaB útvonal aktiválása gyulladásos ingerekkel humán neutrofilekben. Vér. 1997; 89 , 3421–3433. doi: 10.1182/vér.V89.9.3421. [ PubMed ] [ CrossRef ] [ Google Scholar ]88.
Frączek M., Rostkowska-Nadolska B., Kapral M., Szota J., Kręcicki T., Mazurek U. Microarray analysis of NF-κB-dependent genes in chronic rhinosinusitis with nasal polyp. Adv. Clin. Exp. Med. 2013; 22 , 209–217. [ PubMed ] [ Google Scholar ]89.
Jung HJ, Zhang YL, Kim DK, Rhee CS, Kim DY Az NF-κB szerepe az orrpolipokkal járó krónikus rhinosinusitisben. Allergia Asthma Immunol. Res. 2019; 11 , 806–817. doi: 10.4168/aair.2019.11.6.806. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]90.
Sajadimajd S., Khazaei M. Oxidatív stressz és rák: A Nrf2 szerepe. Curr. A rákellenes gyógyszerek céljai. 2018; 18 , 538–557. doi: 10.2174/1568009617666171002144228. [ PubMed ] [ CrossRef ] [ Google Scholar ]91.
London NR, Jr., Tharakan A., Rule AM, Lane AP, Biswal S., Ramanathan M., Jr. A szinonasalis epithelialis sejt barrier funkciójának légszennyező anyagok által közvetített zavara az Nrf2 útvonal aktiválásával megfordul. J. Allergy Clin. Immunol. 2016; 138 :1736–1738.e4. doi: 10.1016/j.jaci.2016.06.027. [ PubMed ] [ CrossRef ] [ Google Scholar ]92.
Tharakan A., Halderman AA, Lane AP, Biswal S., Ramanathan M., Jr. A cigarettafüst-kivonat által kiváltott sinonasalis epithelialis cell barrier diszfunkció megfordítása Nrf2 aktiváción keresztül. Int. Fórum Allergia Rhinol. 2016; 6 , 1145–1150. doi: 10.1002/alr.21827. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]93.
Hudmon A., Schulman H. A többfunkciós Ca2+/calmodulin-dependens protein kinase II szerkezete-funkciója. Biochem. J. 2002; 364 , 593–611. doi: 10.1042/bj20020228. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]94.
Stratton M., Lee IH, Bhattacharyya M., Christensen SM, Chao LH, Schulman H., Groves JT, Kuriyan J. A CaMKII holoenzimek közötti aktiváció által kiváltott alegységcsere elősegíti a kinázaktivitás terjedését. Elife. 2014; 3 :e01610. doi: 10.7554/eLife.01610. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]95.
Erickson JR, Joiner ML, Guan X., Kutschke W., Yang J., Oddis CV, Bartlett RK, Lowe JS, O’Donnell SE, Aykin-Burns N. és társai. Dinamikus út a CaMKII kalcium-független aktiválásához metionin oxidációval. Sejt. 2008; 133 , 462–474. doi: 10.1016/j.cell.2008.02.048. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]96.
Qu J., Mei Q., Niu R. Oxidatív CaMKII mint gyulladásos betegség lehetséges célpontja (Review) Mol. Med. Rep. 2019; 20 , 863–870. doi: 10.3892/mmr.2019.10309. [ PubMed ] [ CrossRef ] [ Google Scholar ]97. Reiter B., Perraudin JP. A laktoferrin és az újszülöttkori E. coli
fertőzések antibakteriális hatása . Szelektív és kritikus áttekintés. Adv. Exp. Med. Biol. 1998; 443 , 175–188. doi: 10.1007/978-1-4757-9068-9_21. [ PubMed ] [ CrossRef ] [ Google Scholar ]98.
Gattas MV, Forteza R., Fragoso MA, Fregien N., Salas P., Salathe M., Conner GE Az oxidatív epiteliális gazdaszervezet védelmét fertőző és gyulladásos ingerek szabályozzák. Free Radic. Biol. Med. 2009; 47 , 1450–1458. doi: 10.1016/j.freeradbiomed.2009.08.017. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]99.
El Hassani RA, Benfares N., Caillou B., Talbot M., Sabourin JC, Belotte V., Morand S., Gnidehou S., Agnandji D., Ohayon R. és társai. A kettős oxidáz2 az emésztőrendszer egészében expresszálódik. Am. J. Physiol. Gasztrointeszt. Liver Physiol. 2005; 288 :G933–G942. doi: 10.1152/ajpgi.00198.2004. [ PubMed ] [ CrossRef ] [ Google Scholar ]100.
Cho DY, Nayak JV, Bravo DT, Le W., Nguyen A., Edward JA, Hwang PH, Illek B., Fischer H. Kettős oxidázok és szekretált citokinek expressziója krónikus rhinosinusitisben. Int. Fórum Allergia Rhinol. 2013; 3 , 376–383. doi: 10.1002/alr.21133. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]101.
Takabayashi T., Schleimer RP Orrpolipok kialakulása: A veleszületett 2-es típusú gyulladás és a fibrin lerakódás szerepe. J. Allergy Clin. Immunol. 2020; 145 , 740–750. doi: 10.1016/j.jaci.2020.01.027. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]102.
Topal O., Kulaksızoglu S., Erbek SS Oxidatív stressz és orrpolipózis: Befolyásolja-e a betegség súlyosságát? Am. J. Rhinol. Allergia. 2014; 28 :e1–e4. doi: 10.2500/ajra.2014.28.3963. [ PubMed ] [ CrossRef ] [ Google Scholar ]103.
Ayala A., Muñoz MF, Argüelles S. Lipid peroxidáció: Malondialdehid és 4-hidroxi-2-nonenál termelése, metabolizmusa és jelátviteli mechanizmusai. Oxidatív Med. Sejt. Longev. 2014; 2014 :360438. doi: 10.1155/2014/360438. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]104.
Schiffrin EL Oxidatív stressz, nitrogén-monoxid-szintáz és szuperoxid-diszmutáz: Az emberi koszorúér-keringés endothel diszfunkciójának hátterében egyensúlyhiány áll. Magas vérnyomás. 2008; 51 , 31–32. doi: 10.1161/HYPERTENSIONAHA.107.103226. [ PubMed ] [ CrossRef ] [ Google Scholar ]105.
Wu MM, Sun H., He GX, Wang TS, Xiao ZQ, Feng XP Differenciálisan expresszált fehérjék meghatározása és jelentősége krónikus arcüreggyulladás, orrpolipok és normál orrnyálkahártya esetén. Zhonghua Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2006; 41 , 171–175. [ PubMed ] [ Google Scholar ]106.
Kwon HS, Bae YJ, Moon KA, Lee YS, Lee T., Lee KY, Kim TB, Park CS, Moon HB, Cho YS Az asztmás betegek perifériás vérének mononukleáris sejtjeiben lévő hiperoxidált peroxiredoxinok összefüggésbe hozhatók az asztma súlyosságával. Life Sci. 2012; 90 , 502–508. doi: 10.1016/j.lfs.2012.01.003. [ PubMed ] [ CrossRef ] [ Google Scholar ]107.
Carnero A., Blanco-Aparicio C., Renner O., Link W., Leal JF The PTEN/PI3K/AKT signaling pathway in cancer, therapy implikations. Curr. A rákellenes gyógyszerek céljai. 2008; 8 , 187–198. doi: 10.2174/156800908784293659. [ PubMed ] [ CrossRef ] [ Google Scholar ]108.
Tanaka Y., Hosoyama T., Mikamo A., Kurazumi H., Nishimoto A., Ueno K., Shirasawa B., Hamano K. A humán kardioszférából származó sejtlapok hipoxiás előkondicionálása fokozza a sejtfunkciókat a PI3K aktiválásával /Akt/mTOR/HIF-1α útvonal. Am. J. Transl. Res. 2017; 9 , 664–673. [ PMC ingyenes cikk ] [ PubMed ] [ Google Scholar ]109.
Yadav UC, Naura AS, Aguilera-Aguirre L., Boldogh I., Boulares HA, Calhoun WJ, Ramana KV, Srivastava SK Az aldose reduktáz gátlás megakadályozza az allergiás légúti remodellinget a PI3K/AKT/GSK3β útvonalon keresztül egerekben. PLoS ONE. 2013; 8 :e57442. doi: 10.1371/journal.pone.0057442. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]110.
Jia M., Chen X., Liu J., Chen J. A PTEN elősegíti a H2O2-vel sérült patkány orrhámsejtek apoptózisát a PI3K/Akt és más utakon keresztül. Mol. Med. Rep. 2018; 17 , 571–579. doi: 10.3892/mmr.2017.7912. [ PubMed ] [ CrossRef ] [ Google Scholar ]111.
Wu MM, Chen T., Xiong W., Huang CJ, Shi ZQ, Pu HJ A PACAP fehérje szerepe krónikus arcüreggyulladásban orrpolipokkal vagy anélkül. Lin Chung Er Bi Yan Hou Tou Jing Wai Ke Za Zhi. 2016; 30 , 1608–1611. doi: 10.13201/j.issn.1001-1781.2016.20.007. [ PubMed ] [ CrossRef ] [ Google Scholar ]112.
Dagli M., Eryilmaz A., Besler T., Akmansu H., Acar A., Korkmaz H. Role of free radicals and antioxidants in nasal polyp. Gégetükör. 2004; 114 , 1200–1203. doi: 10.1097/00005537-200407000-00013. [ PubMed ] [ CrossRef ] [ Google Scholar ]113.
Cheng YK, Tsai MH, Lin CD, Hwang GY, Hang LW, Tseng GC, Shen PS, Chang WC Oxidatív stressz nem allergiás orrpolipokban a bronchiális túlérzékenységgel kapcsolatban. Allergia. 2006; 61 , 1290–1298. doi: 10.1111/j.1398-9995.2006.01228.x. [ PubMed ] [ CrossRef ] [ Google Scholar ]114.
Hariri BM, McMahon DB, Chen B., Freund JR, Mansfield CJ, Doghramji LJ, Adappa ND, Palmer JN, Kennedy DW, Reed DR és társai. A flavonok modulálják a légúti hám veleszületett immunitását: Gyulladáscsökkentő hatások és a T2R14 receptor aktiválása. J. Biol. Chem. 2017; 292 , 8484–8497. doi: 10.1074/jbc.M116.771949. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]115.
Kim SW, Kim DW, Khalmuratova R., Kim JH, Jung MH, Chang DY, Shin EC, Lee HK, Shin HW, Rhee CS és társai. A resveratrol egérmodellben megakadályozza az orrpolipokkal járó eozinofil rhinosinusitis kialakulását. Allergia. 2013; 68 , 862–869. doi: 10.1111/all.12132. [ PubMed ] [ CrossRef ] [ Google Scholar ]116.
Koennecke M., Benecke F., Masche A., Linke R., Bruchhage KL, Pries R., Klimek L., Wollenberg B. Az eNOS fokozott foszforilációja krónikus rhinosinusitisben szenvedő betegek orrpolipjaiban 1,8-kal csökkenthető – cineol. Nitrogén-oxid. 2018; 78 , 89–94. doi: 10.1016/j.niox.2018.06.002. [ PubMed ] [ CrossRef ] [ Google Scholar ]117.
Zhang S., Smith N., Schuster D., Azbell C., Sorscher EJ, Rowe SM, Woodworth BA A kvercetin növeli a cisztás fibrózis transzmembrán konduktancia szabályozó által közvetített kloridtranszportját és a ciliáris ütem gyakoriságát: A krónikus rhinosinusitis terápiás hatásai. Am. J. Rhinol. Allergia. 2011; 25 , 307–312. doi: 10.2500/ajra.2011.25.3643. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]118.
Hoza J., Salzman R., Starek I., Schalek P., Kellnerova R. Az erdostein hatékonysága és biztonságossága orrpolipózissal járó krónikus rhinosinusitis kezelésében – kísérleti tanulmány. Rhinology. 2013; 51 , 323–327. doi: 10.4193/Rhino13.039. [ PubMed ] [ CrossRef ] [ Google Scholar ]119.
Martens S., Mithöfer A. Flavonok és flavon-szintázok. Fitokémia. 2005; 66 , 2399–2407. doi: 10.1016/j.phytochem.2005.07.013. [ PubMed ] [ CrossRef ] [ Google Scholar ]120.
Sato Y., Shibata H., Arai T., Yamamoto A., Okimura Y., Arakaki N., Higuti T. Variation in synergistic activity by flavon and its related compounds on the fokozott susceptibility of different strains of meticillin-rezisztens Staphylococcus aureus a béta-laktám antibiotikumokhoz. Int. J. Antimicrob. Ügynökök. 2004; 24 , 226–233. doi: 10.1016/j.ijantimicag.2004.02.028. [ PubMed ] [ CrossRef ] [ Google Scholar ]121.
Pezzuto JM. A rezveratrol jelensége: A promiszkuitás erényeinek újradefiniálása. Ann. NY Acad. Sci. 2011; 1215 , 123–130. doi: 10.1111/j.1749-6632.2010.05849.x. [ PubMed ] [ CrossRef ] [ Google Scholar ]122.
Csiszar A. Resveratrol gyulladáscsökkentő hatása: Lehetséges szerepe az életkorral összefüggő szív- és érrendszeri betegségek megelőzésében. Ann. NY Acad. Sci. 2011; 1215 , 117–122. doi: 10.1111/j.1749-6632.2010.05848.x. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]123.
Serrano C., Valero A., Picado C. Nazális nitrogén-monoxid. Boltív. Bronconeumol. 2004; 40 , 222–230. doi: 10.1016/S0300-2896(04)75509-X. [ PubMed ] [ CrossRef ] [ Google Scholar ]124.
Juergens UR A monoterpén 1,8-cineol gyulladáscsökkentő tulajdonságai: Jelenlegi bizonyítékok a gyulladásos légúti betegségek együttes gyógyszeres kezelésére. Drug Res. 2014; 64 , 638–646. doi: 10.1055/s-0034-1372609. [ PubMed ] [ CrossRef ] [ Google Scholar ]125.
Xu D., Hu MJ, Wang YQ, Cui YL A kvercetin és annak komplexei antioxidáns hatásai gyógyászati alkalmazásra. Molekulák. 2019; 24 :1123. doi: 10,3390/molekula24061123. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]126.
Cazzola M., Page C., Rogliani P., Calzetta L., Matera MG Multifaceted Beneficial Effects of Erdosteine: More than a Mucolytic Agent. Kábítószer. 2020; 80 , 1799–1809. doi: 10.1007/s40265-020-01412-x. [ PMC ingyenes cikk ] [ PubMed ] [ CrossRef ] [ Google Scholar ]
Vélemény, hozzászólás?